Хронична миелоидна левкемия (ХМЛ)
Ако току що сте научили, че имате или може би имате левкемия, е нормално да се чувствате шокирани и объркани. В текста по-долу може да намерите информация за някои основни понятия, които могат да ви помогнат да научите повече за острата миелоидна левкемия.
Информацията, която ще прочетете не представлява медицински съвети или препоръки и по никакъв начин не замества консултацията и предписанията на лекуващия лекар.
Кръв
За да разберете какво представлява ХМЛ (хронична миелоидна левкемия), първо трябва да научите повече за кръвта. Кръвта е една от течностите в тялото. Състои се от кръвни клетки, които се движат свободно в плазмата. Плазмата е съставена предимно от вода.
Кръвни клетки
Има три основни вида кръвни клетки – червените кръвни клетки (еритроцити), бели кръвни клетки (левкоцити) и кръвните плочици (тромбоцити).
Кръвните клетки имат важни функции. Червените кръвни клетки пренасят кислород в цялото тяло. Белите кръвни клетки помагат в борбата с микроорганизмите. Тромбоцитите контролират кървенето.
Кръвните Ви клетки не са вечни. Много от тях имат кратък живот. Така в тялото Ви през цялото време настъпва подмяна на кръвните клетки.
Образуване на кръвните клетки
Повечето кръвни клетки се образуват в костния мозък. Костният мозък е подобна на гъба тъкан, която се намира във вътрешността на повечето кости.
В костния Ви мозък има кръвообразуващи клетки. Костномозъчните стволови клетки са клетките, от които произлизат всички кръвни клетки. Те се наричат също хемопоетични стволови клетки. Както е показано на Фигура 2, от тях започва родословното дърво на кръвните клетки.
От стволовите клетки се произвеждат нови клетки, които търпят множество промени, за да стигнат до етап на зрели кръвни клетки. Това са клетките-предшественици. За разлика от стволовите, клетките-предшественици са програмирани да продължат зреенето си до точно определен вид кръвни клетки.
Съществуват два вида кръвни клетки-предшественици. Лимфоидните клетки-предшественици дават началото на един от клоновете на родословното дърво. Миелоидните клетки-предшественици дават началото на друг клон.
В края на лимфоидния клон се намира един вид бяла кръвна клетка, наречена лимфоцит. Има три вида лимфоцити. Това са NK клетките, В-клетките и Т-клетките. Лимфоцитите се освобождават от костния мозък в кръвта.
В края на миелоидния клон се намират белите кръвни клетки, червените кръвни клетки и тромбоцитите. Тези бели кръвни клетки се наричат гранулоцити. Гранулоцитите включват неутрофили, еозинофили и базофили. Червените кръвни клетки, тромбоцитите и гранулоцитите се освобождават от костния мозък в кръвта.
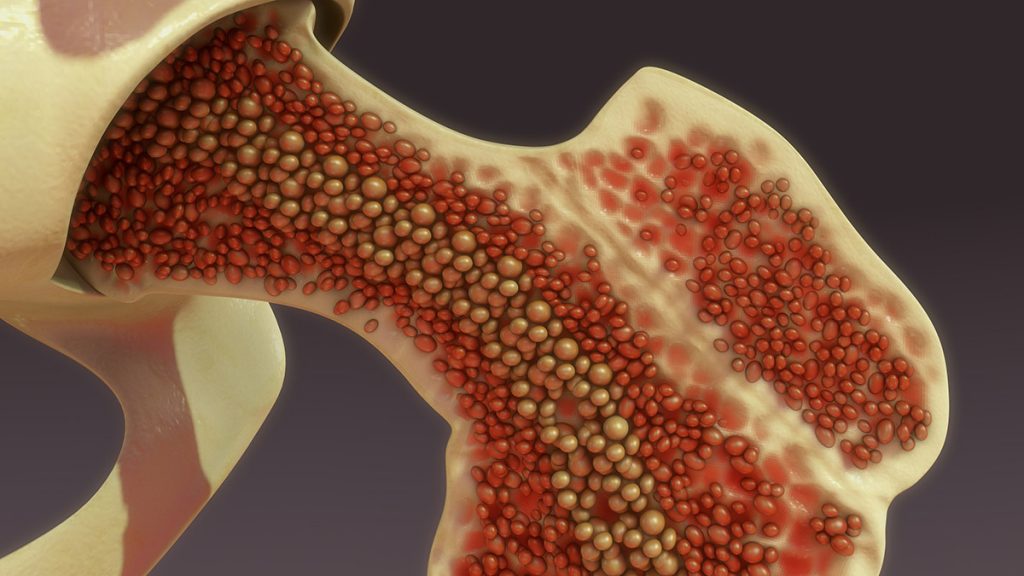
Фигура 1. Костен мозък
Костният мозък е подобна на гъба тъкан, която се намира във вътрешността на повечето кости. Повечето кръвни клетки се образуват в костния мозък.
Заболяване на клетките
Тялото Ви е изградено от трилиони клетки. Ракът е заболяване на клетките. Всеки вид рак е кръстен на здравите клетки, от които произлиза.
Произход на клетката
МПН (миелопролиферативните новообразувания) са група редки кръвни заболявания. Това ракови новообразувания, които произлизат от кръвообразуващите стволови клетки от миелоидния клон. „Миело“ означава костен мозък. „Пролиферативен“ означава растящ и се отнася до образуването на твърде много клетки. Новообразувание е всеки абнормен растеж. При МПН има твърде много кръвообразуващи клетки в костния мозък, което от своя страна е свързано с наличието и на твърде много кръвни клетки.
ХМЛ е вид МПН. При нея е засегната стволовата клетка, която произвежда гранулоцити. По този начин се получава излишък от бели кръвни клетки, по-специално неутрофили. Другите клетки, които могат да бъдат също повишени включват базофили и еозинофили. „Хроничен“ означава, че при този вид рак влошаването настъпва бавно.
Причина за развитие на ХМЛ
Клетките имат контролен център, наречен ядро. Ядрото съдържа хромозоми, които са дълги вериги от ДНК (дезоксирибонуклеинова киселина), плътно обвити около протеини. Вижте Фигура 2. В ДНК са кодирани инструкции за създаването на нови клетки и контрола на тяхната функция. Тези инструкции се наричат гени
В гените на раковите клетки се наблюдават промени, наречени мутации. Мутациите са причината раковите клетки да не функционират като здравите клетки. Също така, мутациите са причината раковите клетки понякога да изглеждат много различно от нормалните клетки. Мутацията, която причинява ХМЛ се нарича BCR-ABL1 ген. Тя е обяснена по-долу.
Гените са малки частици ДНК.
Всяка клетка трябва да произведе копие на своите хромозоми преди да се раздели на 2 нови клетки. Понякога обаче се получават грешни копия. Един вид грешка настъпва когато части от две хромозоми се разменят една с друга. Това се нарича транслокация. Тя може да е причината за образуване на слети гени (фузионни гени).
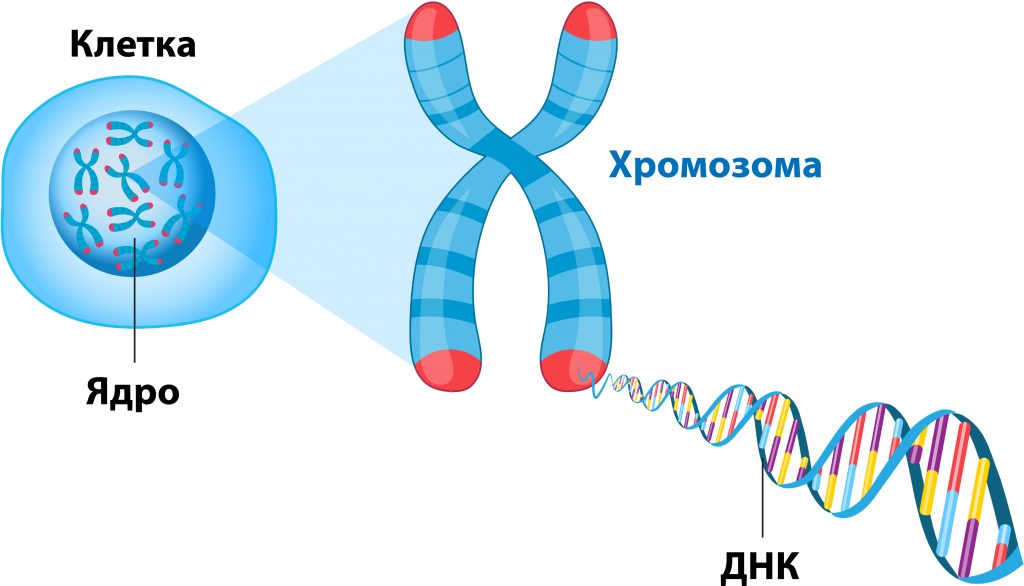
Фигура 2. Генетичен материал в клетките
Повечето човешки клетки съдържат в себе си информация – план, наречен „план на живота“. Той представлява план за това как са създадени и работят телата ни. Той се намира в хромозомите. Хромозомите са дълги нишки от ДНК, които са плътно обвити около белтъци. Гените са малки парчета ДНК. Хората имат около 20 000 до 25 000 гена.
BCR-ABL1 е фузионен ген.Той не може да бъде намерен в здравите кръвни клетки. Не се предава от родители на деца. Той кодира протеин, който предизвиква образуването на прекалено много гранулоцити. Тези гранулоцити са по-различни.Те не узряват и не умират като нормалните клетки..
BCR-ABL1 се образува чрез транслокация между хромозоми 9 и 22.
В хромозома 9 се съдържа гена ABL. По време на транслокацията, ABL гена се прикрепя към хромозома 22. Тази абнормна хромозома 22 се нарича Филаделфийска хромозома.
ФИЛАДЕЛФИЙСКА ХРОМОЗОМА
Филаделфийската хромозома е отличителният белег на ХМЛ. Тя съдържа гена BCR-ABL1. Ако нямате Филаделфийска хромозома или гена BCR-ABL1, това означава, че нямате типична ХМЛ.
Три фази
ХМЛ протича в три фази. Те се наричат хронична, ускорена и бластна фаза. Те се определят от броя на бластите в кръвта и костния мозък.
Бластите са ранните форми на кръвните клетки. Те са стволови клетки, които не могат да се превърнат в здрави, зрели клетки.При повечето случаи на ХМЛ не се наблюдават голям брой бласти. Високият брой на бластите е знак за по-напреднала фаза на ХМЛ.
Хронична фаза
Първата фаза на ХМЛ се нарича хронична фаза. В тази фаза се наблюдава увеличен брой на белите кръвни клетки в кръвта, костния мозък или в двете.По-малко от 10 от всеки 100 кръвни клетки са бласти (<10%).
Най-често в хроничната фаза липсват симптоми на заболяването. При наличието им, те са най-често леки. Може да чувствате умора. Може да имате усещане за тежест под ребрата вляво. Тялото Ви все още може да се бори с микроорганизмите, тъй като броя на кръвните клетки е близък до нормалния.
В хроничната фаза ХМЛ прогресира много бавно. Може да изминат няколко месеца или години докато премине в следващата фаза. В сравнение с другите фази, когато е в хроничната фаза ХМЛ показва тенденция за по-добър отговор на лечението.
Ускорена фаза (фаза на акцелерация)
Втората фаза на ХМЛ се нарича фаза на акцелерация. В тази фаза броят на бластите е значимо по-голям. Броят на белите кръвни клетки е също е увеличен.Може да се наблюдава и много малък брой тромбоцити в кръвта.
Във всички фази, клетките на ХМЛ съдържат Филаделфийска хромозома. Въпреки това, във фазата на акцелерация могат да настъпят нови промени в хромозомите.
В тази фаза, клетките на ХМЛ могат да растат бързо. Може да имате симптоми. Такива симптоми включват висока температура, загуба на тегло без спазване на диета и загуба на апетит. Може да имате и увеличен далак.
Бластна фаза
Третата и последна фаза на ХМЛ се нарича бластна фаза. Също така се нарича и „бластна криза“. Веднъж преминала в бластната фаза ХМЛ може да бъде животозастрашаващо състояние.
В бластната фаза броят на бластите е много голям. Бластите може да са се разпространили извън кръвта или костния мозък в други тъкани. Симптомите са чести. Те могат да включват инфекции, кървене, болки в корема и болки в костите.
Клетките на ХМЛ стават все по-абнормни. Те често функционират като при остра левкемия. Острата левкемия се влошава много бързо. Видовете остра левкемия са ОМЛ (остра миелоидна левкемия) и ОЛЛ (остра лимфобластна левкемия).
Медицинска история
Вашата медицинска история включва всички Ваши здравословни проблеми и лекарствата, които сте приемали в рамките на целия Ви живот. Ще бъдете попитани какви заболявания, травми, здравословни проблеми сте имали. Може да бъде полезно да направите списък със старите и нови лекарства, които приемате.
Някои видове рак и други здравословни състояния се предават в семейството. Поради това Вашият лекар ще попита за медицинската история на близките Ви кръвни роднини. Вашият лекар може да попита за здравословното състояние на на Вашите братя и сестри, родители, баби и дядовци и техните роднини. Имайте готовност да кажете кой от какви заболявания и на каква възраст е боледувал.
Медицинската история е необходима за диагностиката и планиране на лечението
Физикален преглед
Лекарите често провеждат и физикален преглед заедно с получаването на медицинската история. Физикалният преглед е изследване на Вашето тяло за признаци на заболяване. Първоначално ще бъдат измерени основните функции на тялото Ви. Тези функции включват Вашата температура, кръвно налягане и пулс и дихателна (респираторна) честота. Теглото Ви също ще бъде измерено.
По време на прегледа Вашият лекар ще преслуша белите дробове, сърцето и корема Ви.Вашият лекар също ще прегледа и също ще прегледа и други части на тялото Ви. Това се налага, за да се прецени дали органите са с нормални размери, дали са меки или твърди и дали са болезнени при докосване.
Ракът и някои други състояния могат да предизвикат уголемяване и втвърдяване на органите. При ХМЛ далакът ви може да е с по-големи от нормалните размери. Далакът е малък орган, който се намира вляво от стомаха ви. Той филтрира кръвта, съхранява кръвните клетки и унищожава старите кръвни клетки.
Кръвни изследвания
Кръвните изследвания могат да бъдат от полза за диагностициране на ХМЛ. Те могат да помогнат за откриването и на други заболявания. За провеждане на кръвно изследване е необходима проба от кръвта Ви. Кръвните проби могат да бъдат получени чрез изтегляне на кръв.
Вземане на кръв
При някои кръвни изследвания се изисква да не сте приемали храна и вода няколко часа преди изследването. Кръвните проби ще бъдат взети от вената Ви с игла. Вашата кръвна проба ще бъде изпратена в лаборатория. Там лекар- патолог, хематолог или лекар клинична лаборатория ще проведе кръвните изследвания. Патологът е лекар, който е експерт в изследването на клетките за откриване на наличието на заболяване.
ПКК с диференциално броене
С ПКК (пълна кръвна картина) се определят съставките на кръвта. Често се извършва апаратно. Резултатите от изследването показват броя на белите кръвни клетки, червените кръвни клетки и тромбоцитите. При наличие на рак и други здравословни проблеми може да се наблюдава нисък или висок брой на тези кръвни клетки. Това е основно изследване, което дава информация за цялостното Ви здравословно състояние.
Има няколко вида бели кръвни клетки. С диференциалното броене се определя броя на всеки вид клетки и съотношението между тях. Чрез това изследване Вашият лекар може да определи причината за отклонението в белите кръвни клетки.
Биохимичен профил
Химичните съединения се отделят в кръвта Ви от черния дроб и други органи. Биохимичният профил отразява нивата на тези вещества. Отклоненията в резултатите може да са знак, че някой от органите или системите в тялото Ви не функционират добре. Тези органи включват черния дроб и бъбреците. Това изследване може да бъде повторено отново по време и след лечението за оценка на резултатите.
Изследване на костен мозък
Изследването на костен мозък се извършва чрез вземане на клетки от костния Ви мозък. Резултатите от изследването ще бъдат използвани за определяне на фазата на заболяването. Изследването на костен мозък може да се проведе и по време на лечението, за да се оценят резултатите от него.
Аспирация и биопсия
Изследването на костен мозък включва две процедури. С аспирацията на костен мозък се получава малко количество течен костен мозък. Костномозъчната биопсия осигурява проба от костта и самия костен мозък.
Често тези процедури се извършват едновременно. Пробите се получават от задната част на тазобедрената кост. Преди това може да Ви бъде дадено леко успокоително лекарство.
Най-често ще бъдете поставен да легнете на една страна, както е показано на Фигура 3. Някои хора лежат по корем. Вашият лекар първо ще почисти и обезболи кожата Ви.
При провеждането на аспирация през кожата Ви ще бъде вкарана куха игла и ще бъде натисната до костта. След това ще се изтегли малко количество течен костен мозък в спринцовка. При биопсията в костта Ви ще бъде поставена по-широка игла и със завъртане ще се получи проба от сърцевината на костта. Може да чувствате болка в костта по време и няколко дни след процедурите. По кожата Ви може да се получат синини.
Лабораторни изследвания
Пробите ще бъдат изпратени в лаборатория за изследване. Лекар-патолог ще изследва пробите с микроскоп. Той или тя ще оцени броя и вида на клетките. Тази информация ще се използва за определяне на фазата на ХМЛ. Ще бъдат направени и генетични изследвания.
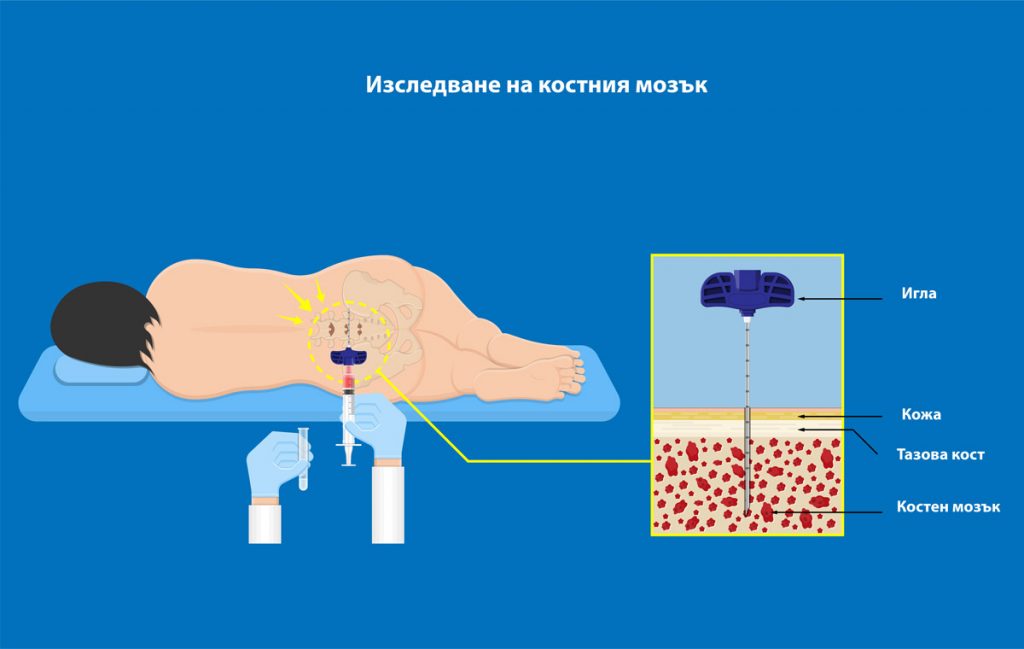
Фигура 3. Изследване на костен мозък
При изследването на костен мозък се получава проба от кост и костен мозък. Пробите се получават от задната част на тазобедрената кост.
Генетични изследвания
При ХМЛ се провеждат генетични изследвания на левкемични клетки. Те оценяват за за различни промени в гените и хромозомите. Такива промени липсват при раждането. Генетичните тестове се извършват от патолози и генетици. Често са необходими няколко дни, преди да се получат резултатите от лабораторията.
Цитогенетично изследване на костен мозък
Цитогенетиката изследва хромозомите. Използва се за потвърждаване на ХМЛ чрез изследване за наличие на Филаделфийска хромозома. Лекарят- патолог или генетик ще изследва и за други промени в хромозомите. Това ще помогне да се определи фазата на ХМЛ.
Цитогенетичното изследване може да се използва и за оценка на резултатите от лечението. Ако изследването покаже липса на абнормните хромозоми се смята, че лечението ефективно. Абнормните хромозоми се появяват отново, когато по някаква причина лечението стане неефективно.
Кариотип
Кариотипът представлява изображение на хромозомите в клетките. Вижте Фигура 6. При ХМЛ трябва да бъде използвана проба от костен мозък. Към пробата се добавят химични съединения, за да се стимулира растежа на клетките. След това клетките ще бъдат изследвани с микроскоп.
Фигура 6 Кариотип
Кариотипът е изображение на хромозомите в клетките. То показва наличието на абнормни промени в хромозомите.
FISH
Ако не може да се определи кариотипа може да се извърши изследването FISH (флуоресцентна in situ хибридизация). С FISH може да изследва за наличие на BCR-ABL1 гена, за да се потвърди ХМЛ. Ако не могат да бъдат направени други изследвания FISH може да се използва и за оценка на отговора на лечението.
При FISH се използват специални цветни бои, наречени сонди. Сондите се прикрепят към BCR гена и ABL гена. BCR-ABL1 генът се открива, когато цветовете на сондите се припокриват. Това изследване може да се извърши с костен мозък или с кръвна проба.
QPCR-IS
QPCR (количествен анализ на обратна транскриптаза-полимеразна верижна реакция) е изследване, което се използва за оценка на BCR-ABL1 гена. Може да се извърши с проба от кръв или костен мозък. Смята се за много чувствителен метод. Чрез него може да се открие наличието на една ХМЛ клетка сред повече от 100 000 здрави клетки.
Препоръчва се да се използва лаборатория, която работи с IS (международна скала). IS е стандартизиран метод за измерване и отчитане на QPCR резултатите. Ако не може да се използва IS е по-трудно да се сравнят получените в различни лаборатории резултати. В този случай се препоръчва за сравнение да се използват резултатите от същата лаборатория. Прочетете страница 29, за да научите повече за IS.
Изследване за хепатит
Наличието на хепатит В може да бъде важен фактор при определяне на лечението на ХМЛ. Раковото заболяване или противораковото лечение могат да активират отново Хепатит В. Съобщете на лекуващия екип ако сте заразен с хепатит. Ако не сте сигурни, се препоръчва да се изследвате. Необходима е кръвна проба за провеждане на изследването.
Тук са описани основните видове терапии при ХМЛ. Познаването им ще Ви помогне да разберете възможностите за лечение. Прилагат се повече от един медикамент при ХМЛ. Не всеки получава всички видове лекарства, описани тук.
Информацията, която ще прочетете не представлява медицински съвети или препоръки и по никакъв начин не замества консултацията и предписанията на лекуващия лекар.
Тирозин киназни инхибитори
В Ръководство 2 са изброени различните ТКИ (тирозин киназни инхибитори), използвани за лечение на ХМЛ. Те представляват стандартното лечение. ТКИ принадлежат към клас лекарства, наречени прицелна терапия. Тези лекарства действат върху молекулите, определящи растежа на раковите клетки. Много прицелни терапии спират сигналите, стимулиращи растежа на клетките.
Как действат ТКИ
Протеинът, който се произвежда от BCR-ABL1 гена е тирозин киназа. Той премества определени химични съединения наречени фосфати от една молекула в друга. След това фосфатът „задейства“ следващата молекула в сигналния път. ТКИ блокират прехвърлянето на фосфатите, което от своя страна спира сигналите за растеж. Вижте ТКИ се различават малко по начина си на действие. Може да се започне с едно лекарство, което обаче може да не действа или да спре да действа с течение на времето. Последното се случва често, когато настъпи нова мутация в клетките на ХМЛ. Тогава може да се преминаване към различен ТКИ с действие срещу новата мутация.
Иматиниб
Иматиниб е първият ТКИ, одобрен от американската Агенцията за контрол на храните и лекарствата за лечение на ХМЛ. Затова се нарича ТКИ от първо поколение. Той се свързва с неактивното място на протеина BCR-ABL1 и спира сигналите за растеж.
Дазатиниб
Дазатиниб е второ поколение ТКИ. Дазатиниб е по-мощен от иматиниб. Той се свързва с активните и неактивни части на протеина BCR-ABL1 и блокира сигналите за растеж. Действа срещу повечето мутации на BCR-ABL1. Той също така блокира SCR, PDGFR и KIT киназите.
Нилотиниб
Нилотиниб е второ поколение ТКИ. Той действа почти по същия начин като иматиниб. Въпреки това, нилотиниб е по-мощен. Действа срещу повечето мутации на BCR-ABL1. Той също така блокира PDGFR и KIT киназите.
Ръководство 2. ТКИ за ХМЛ
| Генерично (химическо) наименование | Търговско име (продава се с това име) | Поколение |
Иматиниб | Gleevec® | Първо |
Дазатиниб | Sprycel® | Второ |
Нилотиниб | Tasigna® | Второ |
Бозутиниб | Bosulif® | Второ |
Понатиниб | Iclusig® | Трето |
Бозутиниб
Бозутиниб е второ поколение ТКИ. Той се свързва с активните и неактивни части на протеина BCR-ABL1 и блокира сигналите за растеж. Действа срещу повечето BCR-ABL1 мутации. Блокира също и SCR киназите.
Понатиниб
Понатиниб е трето поколение ТКИ. Той блокира много тирозин кинази, включително BCR-ABL1. Той действа срещу всички BCR-ABL1 мутации, включително T315I.
Какво да очаквате
Различните ТКИ използвани за лечение на ХМЛ са сходни в много отношения. Те се произвеждат под формата на хапче, което се приема през устата. По време на лечението ще трябва да избягвате определени лекарства, храни и напитки, като например сок от грейпфрут. Попитайте Вашия лекар за повече информация за това как да приемате ТКИ.
Странични ефекти
Страничният ефект представлява нарушено здравословно състояние или неприятно физическо или емоционално усещане, причинено от дадено лекарство. Не всеки човек получава еднакви странични ефекти. Страничните ефекти зависят от лекарството, приеманото количество, продължителността на лечението и характеристиките на човека, който го приема.
Някои нежелани реакции са чести при лечение с ТКИ. Те включват ниски стойности на кръвните показатели. В резултат на това може да почувствате гадене, диария и повръщане. Може да се появят промени в кожата Ви, като обрив. Може да почувствате умора, главоболие и втрисане. Може да се задържат течности в крайниците или около определени органи.
Всички ТКИ могат да причинят тежки странични ефекти. Вашият лекар ще следи за безопасността на лечението Ви. Тежките странични ефекти включват сърдечни проблеми, отклонения в чернодробната функция и бъбречна недостатъчност. Не приемайте ТКИ по време на бременност или кърмене.
Не всички странични ефекти на ТКИ са изброени тук. Моля, попитайте Вашия лекуващ лекар за пълния списък на по-честите и редки нежелани реакции. Ако някой страничен ефект ви притеснява, кажете на лекуващия си лекар. Може да има начин да ви се помогне да се почувствате по-добре. Има и начини за предотвратяване на някои странични ефекти.
Химиотерапия
Химиотерапията включва лекарства, които нарушават жизнения цикъл на раковите клетки. Различните видове химиотерапия се различават по своя механизъм на действие. Някои видове унищожават раковите клетки като увреждат тяхната ДНК или нарушават образуването на ДНК. Други действат върху определени части от клетката, които са необходими за образуването на нови клетки. По този начин не се произвеждат нови клетки, които да заменят умиращите клетки. Химиотерапията може да действа както върху раковите, така и върху нормалните клетки.
Някои химиотерапивтици действат в активната фаза на растеж на клетките.
Какво да очаквате
Химиотерапията може да включва едно или повече лекарства. Когато се използва само едно лекарство, се нарича монотерапия. Не всички лекарства обаче действат по един и същи начин, затова често се използва повече от едно лекарство. Комбинираното лечение включва използването на два или повече химиотерапевтика.
Омацетаксин е най-новата химиотерапия за ХМЛ. Активен е срещу всички мутации, които могат да са причина за липсата на ефект от ТКИ. Използва се в напредналите фази на ХМЛ.
Омацетаксин се прилага под формата на течност, която се инжектира подкожно с игла. Някои други химиотерапевтици също се инжектират венозно. Или да се дават като хапче през устата.
Химиотерапията се прилага под формата на цикли, в които се прилага лекарството, последвани от дни на почивка. Това позволява на тялото Ви да се възстанови преди следващия цикъл. Циклите се различават по своята продължителност в зависимост от това кои лекарства се използват. Често цикълът е дълъг 14, 21 или 28 дни. Ако Ви предстои химиотерапия, попитайте Вашия лекар колко цикъла ще Ви бъдат приложени. Попитайте също колко дни ще приемате лечение в рамките на един цикъл.
Странични ефекти
Страничните ефекти на химиотерапията зависят от множество фактори. Тези фактори включват вида на лекарството, дозата, продължителността на лечението и характеристиките на човека, който го приема. Като цяло страничните ефекти настъпват в резултат от смъртта на бързорастящите клетки.
Бързорастящите клетки се намират в космените фоликули, червата, устната кухина и кръвта. Смъртта на тези клетки може да причини нисък брой на кръвните клетки, загуба на апетит, гадене, повръщане, диария, косопад и язви в устата.
Повечето странични ефекти се появяват скоро след започване на лечението и спират след края му. Други странични ефекти обаче са дългосрочни или могат да се появят години по-късно. Късните странични ефекти включват включват развитието на друг вид рак, сърдечни заболявания и проблеми със забременяването (безплодие).
Не всички странични ефекти на химиотерапията са изброени тук. Моля, попитайте Вашия лекуващ лекар за пълен списък на по-честите и редки нежелани реакции. Ако даден страничен ефект Ви притеснява, кажете на лекуващия си лекар. Може да има начини да ви се помогне да се почувствате по-добре. Има и начини за предотвратяване на някои странични ефекти.
- Информацията за лекарственото лечение е адаптирана по NCCN Patient Guideline “Chronic Myeloid Leukemia” v.2018. Някои от терапиите може да не са налични в България.
Трансплантацията на хемопоетични клетки
Костномозъчните стволови клетки са клетки, от които се образуват всички кръвни клетки. Те се намират главно в костния мозък. Ракът или неговото лечение може да увреди или унищожи кръвните стволови клетки.
Трансплантацията на стволови клетки замества увредените или унищожени стволови клетки със здрави стволови клетки. При алогенна трансплантация на стволови клетки се използват здрави стволови клетки от донор. Не е задължително донорът бъде Ваш роднина. Тази трансплантация се нарича още алогенна НСТ (трансплантация на хемопоетични клетки).
Здравите стволови клетки ще дадат началото на нови костномозъчни и кръвни клетки. Така се създава нова имунна система. Друго предимство на тази трансплантация е ефектът GVL (реакция на присадката срещу левкемията). GVL ефектът е атакуването на раковите клетки от трансплантираните стволови клетки. Следва кратко описание са стъпките на алогенната НСТ.
HLA типизиране
Трябва да се направи специално изследване, за да се намери най-подходящият за Вас донор. За да има ефект от това лечение трябва да е на лице почти перфектно съвпадение между донорския и Вашия тип тъкан. Изследването, което се използва за оценка на тъканната съвместимост, се нарича HLA (човешки левкоцитен антиген) типизиране. За извършване на изследването е необходима кръвна проба.
Кондициониране
Преди трансплантацията ще бъдете подложени на лечение, което унищожава клетките на костния мозък. Смъртта на тези клетки създава място за здравите стволови клетки. То също така отслабва и имунната Ви система, за да не реагира тялото срещу трансплантираните клетки.
Има два основни вида кондициониращо лечение. Високодозовото кондициониране се състои в прилагане на високи дози силна химиотерапия. Кондиционирането с по-ниска интензивност се състои в ниски дози силна химиотерапия. Може да се приложат и лекарства с ниска интензивност. Лъчетерапията може също да бъде назначена като част от кондициониращото лечение.
Високодозовото кондициониране може да причини много тежки странични ефекти. Може дори да е смъртоносно. Освен това не всеки го понася. Вашият лекар ще реши дали сте достатъчно здрави за това лечение. Кондиционирането с намалена интензивност може да се използва при по-възрастни или увредени като цяло хора. В тези случаи обаче вероятността за рецидив на рака е по-голяма.
Трансплантация на стволови клетки
След химиотерапията ще получите здравите стволови клетки чрез преливане. Преливането (трансфузията) представлява бавно инжектиране на кръвни продукти през централнен източник в голяма вена. Централният източник (или централен венозен катетър) представлява тънка тръбичка. Тя ще бъде вкарана през кожата Ви чрез един разрез и във вената Ви чрез втори разрез. Използва се локална упойка. Тази процедура може да отнеме няколко часа.
Трансплантираните стволови клетки ще се придвижат до костния Ви мозък, където ще започнат да нарастват. Ще се образуват нови, здрави кръвни клетки. Това се нарича присаждане. Обикновено отнема около 2 до 4 седмици.
Дотогава няма да имате почти никаква имунна защита. Може да се наложи да останете в много чиста стая в болницата. Може да Ви бъдат назначени антибиотици за предотвратяване или лечение на инфекция. Може да Ви бъде проведено и преливане на червени кръвни клетки за предотвратяване на кървене и за лечение на анемия. Може да се проведе преливане на тромбоцити за лечение на ниския брой на тромбоцитите или при кървене. Докато чакате да се присадят клетките, е вероятно да се чувствате уморени и слаби.
- Информацията е адаптирана по NCCN Patient Guideline “Chronic Myeloid Leukemia”v.2018.
Текстът е прегледан от д-р Доротея Тодориева, УМБАЛ „д-р Георги Странски“, гр. Плевен
Информацията е адаптирана по NCCN Patient Guideline “Chronic Myeloid Leukemia” v.2018.
Текстът е прегледан от д-р Доротея Тодориева, хематолог в УМБАЛ „д-р Георги Странски“, гр. Плевен
